2015年福建省福州市中考化学试题(word版)
2015年福建省福州市中考化学试题(word版)
2015年福州市初中毕业会考、高级中等学校招生考试
化学试卷
可能用到的相对原子质量:H―1 C―12 N―14 O―16 Na―23 Ca―40
一、选择题(共36分)
1.下列有关“化学与生活”的认识不科学的是( )
A.天然气是应用广泛的燃料
B.吃水果和蔬菜可以补充维生素
C.可以食用甲醛溶液浸泡的海产品
D.可降解塑料的问世减少了白色污染
2.二氧化钛(TiO2)可作水分解的光催化剂,其中氧元素为―2价,则钛元素的化合价为( )
A.+1 B.+2 C.+3 D.+4
3.根据图1的信息判断,下列关于铝的说法错误的是( )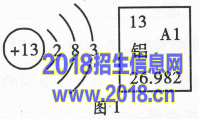
A.属于金属元素
B.原子的核电荷数是13
C.相对原子质量是26.982g
D.在化学反应中,原子易失去电子形成Al3+
4.下列化学式表示的物质是某化学肥料的主要成分,其中属于复合肥料的是( )
A.O2- ―氧离子 B.3H―3个氢元素
C.Fe3 O4 ―四氧化三铁 D.2N2―2个氮气分子
5.实验结束后,图2中仪器的处理方式正确的是( )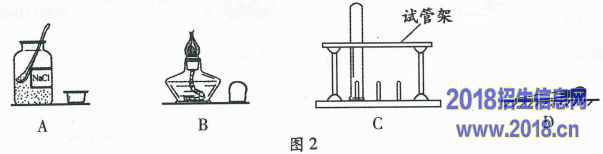
6.市场上有“加碘食盐”、“高钙牛奶”、“含氟牙膏”等商品,这里的“碘、钙、氟”指的是( )
A. 单质 B. 元素 C. 分子 D. 原子
7.下列关于水的说法正确的是( )
A.所有物质都易溶于水 B. 可将工业废水任意排入内河
C. 生活中常用肥皂水检验软水和硬水 D. 水电解过程与电源正极连接的一端产生氢气
8.几种常见物质的pH范围如表1,其中酸性最强的是( )
|
物质 |
酸奶 |
鸡蛋清 |
牙膏 |
肥皂水 |
|
pH范围(常温) |
4~5 |
7~8 |
8~9 |
10~11 |
A.酸奶 B.鸡蛋清 C.牙膏 D.肥皂水
9.图3是某物质的分子模型,下列关于该物质说法正确的是( )
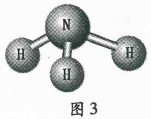 A.属于有机物
A.属于有机物
B.化学式为NH3
C.氮元素和氢元素的质量比为3:1
D.氢元素的质量分数= 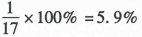
10.下列应用与中和反应原理无关的是( )
A.用浓硫酸干燥湿润的氧气 B.用熟石灰改良酸性土壤
C.服用含氢氧化铝的药物治疗胃酸过多 D.用氢氧化钠溶液洗涤石油产品中的残留硫酸
11. 下列鉴别物质所用的方法或试剂,错误的是( )
A.氧气和氮气――观察颜色 B.铁粉和碳粉――用稀硫酸
C.羊毛和化学纤维――点燃闻气味 D.氢氧化钠溶液和水――用酚酞溶液
12. 实验室用硝酸钾固体配制100.0g溶质质量分数为3.0%的硝酸钾溶液,下列说法正确的是( )

A.用50mL量筒量水
B.将固体放于托盘天平的右盘称取
C.将固体直接投入量筒中溶解
D.将配制好的溶液装入贴有标签(如图4)的试剂瓶中,塞好瓶塞
二、非选择题(共64分)
13.(14分)多角度认识物质的变化,有助于我们更好地理解化学知识。
(1)从微观角度(图5为某化学反应的微观示意图,据图回答下列问题)
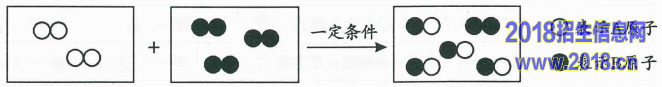
①微观上看,该化学变化中发生根本改变的微粒是 (填 “原子”或“分子”),变化过程中,同种原子的个数 (填“有”或“没有”)增减。。
②参加反应的A2与B2两种物质的分子个数比为 。
(2)从反应类型角度(一种物质可通过不同的反应类型生成,以二氧化碳为例)
①能与氧气化合生成二氧化碳的物质是 (填一种物质化学式)。
②高温下,石灰石分解生成二氧化碳的化学方程式是 。
③在一定条件下,碳与铁的氧化物能发生置换反应,生成二氧化碳和 (填化学式)。
 (3)从能量变化角度(借用途6装置分别进行下列实验,认识物质变化中的能量变化)
(3)从能量变化角度(借用途6装置分别进行下列实验,认识物质变化中的能量变化)
①往烧杯中加入一定量生石灰会引起白磷燃烧,从燃烧条件分析,此时生石灰的作用是 。写出生石灰与水反应的化学方程式
。
②将一定量的下列某物质溶于烧杯中的冷水,其中能引起白磷燃烧的是 (填标号)。
A.氯化钠 B. 硝酸铵 C. 浓硫酸 D. 氢氧化钠
14、(10分)“比较归纳法”是学习化学的一种重要方法。( “―”表示相连的两种物质能发生反应,“→”表示某种物质可通过一步反应转化为另一种物质。)
(1)请以表2中序号Ⅰ为示例,填写序号Ⅱ、Ⅲ中的空格:
|
项目 序号 |
举例 |
物质类别间的相互反应 |
物质类别间的转化 |
|
Ⅰ |
CaCl2+Na2CO3= CaCO3↓+2NaCl |
盐1―盐2 |
盐→新盐 |
|
Ⅱ |
写出硫酸与氯化钡反应的化学方程式
|
酸―盐 |
酸→ |
|
Ⅲ |
写出氢氧化钠转变为另一种碱的化学方程式 |
碱― |
碱→新碱 |
表2
(2)室温下,氯化镁与下列物质的变化关系,正确的是 (填标号)。
A.MgCl2―AgNO3 B. KNO3→MgCl2 C. MgCl2―HCl D. Mg(OH)2→MgCl2
15、(10分)分析处理图表中的信息是学习化学的一种重要方法。
(1)表3是氯化钠和碳酸钠在不同温度时的溶解度,根据此表回答:
|
温度/℃ |
10 |
20 |
30 |
40 |
|
|
溶解度/g |
氯化钠 |
35.8 |
36.0 |
36.3 |
36.6 |
|
碳酸钠 |
12.2 |
21.8 |
39.7 |
53.2 |
|
表3
①40℃时,氯化钠的溶解度为 g。
②碳酸钠的溶解度随温度的升高而 (填“增大”或“减少”)。在20℃时,将100g的水加入30g碳酸钠中,充分搅拌后得到的是 (填“饱和溶液”或“不饱和溶液”),将上述溶液升温到30℃,该溶液的溶质质量分数为 (计算结果精确到0.1%)。
③10℃时,分别配制表中两种物质的饱和溶液,其中溶质质量分数较小的物质是 。
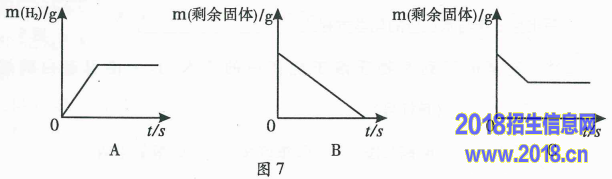
(2)将足量的稀盐酸加入一定量的铁、铜混合物中,写出其中反应的化学方程式
。图7是实验过程生成气体或剩余固体的质量随反应时间的变化关系,其中表示正确的是 (填标号)。
16、(16分)实验室利用图8实验装置进行有关化学实验,回答下列问题:
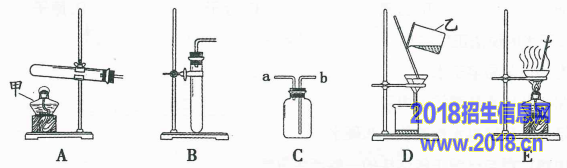
(1)写出图8中仪器甲、乙的名称:甲 ,乙 。
(2)实验室用高锰酸钾制取氧气,发生装置可选择图8中的 (填标号),写出该反应的化学方程式 。用充满水的装置C收集氧气,则氧气需从 (填
“a” 或“b”)端通入。
(3)实验室制取二氧化碳的化学方程式 ,用装置C收集二氧化碳,验满时,燃着木条应放在 (填“a” 或“b”)端,检验二氧化碳的试剂是 。
(4)用上述制取二氧化碳实验后的固液残留物进行过滤、蒸发的操作训练。
①对固液残留物进行过滤,应选择图8中 (填标号)装置,过滤时玻璃棒的作用是
。
②取上述少量滤液进行蒸发,蒸发过程玻璃棒不断搅拌的目的是 ,析出的固体中一定含有的物质是 。
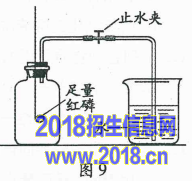
17、(10分)空气中氧气含量测定的再认识。
【实验回顾】图9是实验室用红磷燃烧来粗略测定空气中氧气含量的装置。
(1)写出红磷燃烧的化学方程式 。
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内 减少,烧杯中水倒吸到集气瓶。若装置的气密性良好,操作规范,用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量。
 【问题提出】有实验资料表明:燃烧过程中当氧气体积分数低于7%时,红磷就无法继续燃烧,因此通过上述实验,测量结果与理论值误差较大。
【问题提出】有实验资料表明:燃烧过程中当氧气体积分数低于7%时,红磷就无法继续燃烧,因此通过上述实验,测量结果与理论值误差较大。
【实验改进】
Ⅰ. 根据铁在空气中生锈的原理设计图10实验装置,再次测定空气中氧气含量。装置中饱和食盐水、活性炭会加速铁生锈。
Ⅱ.测定实验数据如表4
|
测量 项目 |
实验前 |
实验后 |
|
|
烧杯中水的体积 |
烧杯中剩余水的体积 |
集气瓶(扣除内容物)和导管的容积 |
|
|
体积/mL |
80.0 |
54.5 |
126.0 |
表4
【交流表达】
⑴铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化铁[Fe(OH)2],写出该反应的化学方程式 。
⑵根据表4数据计算,改进实验后测得的空气中氧气的体积分数是 (计算结果精确到0.1%)。
⑶从实验原理角度分析,改进后的实验结果比前者准确度更高的原因是:
① ;
② 。
18.(4分)某碳酸钠样品中混有少量氯化钠,根据图11所示信息计算该样品中碳酸钠的质量分数。(计算结果精确到0.1%)(反应的化学方程式:CaCl2+Na2CO3= CaCO3↓+2NaCl)
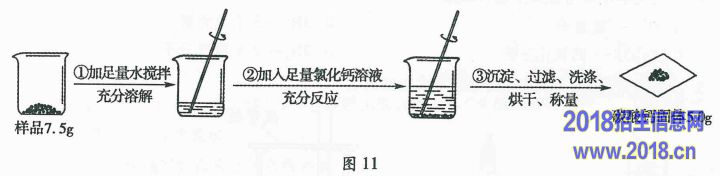


更多2015年中考试题及答案查询请点击:http://www.zspx.cn/news-id-8538.html (全国各地2015中考试题及答案下载汇总)

